传统的癌症治疗手段包括手术、化疗和放疗,该方法往往针对性较差,在杀死肿瘤细胞的同时,也会损伤正常细胞,从而产生一系列的副作用。单克隆抗体是肿瘤靶向治疗的有力工具,但是由于单克隆抗体分子较大(约150kDa),限制了它们进入致密肿瘤组织中的隐蔽表位,并可能损害治疗效果。此外,单克隆抗体的半衰期较长可能导致安全问题,进一步限制其在成像或放射免疫治疗等领域的应用。单域抗体(sdAbs)最初在骆驼科动物或鲨鱼中发现,通常称为纳米抗体或VNAR,已成为传统治疗性抗体的有前途的替代品。sdAbs具有许多优异的物理化学和药理学特性,包括体积小、溶解性和热稳定性好、表位更容易接近以及组织穿透性强。sdAbs的动物来源所固有的挑战限制了它们在临床上的使用。近年来,已经开发出各种创新的人源化技术,包括互补决定区(CDR)移植或全人源sdAbs的完全工程化,以减轻潜在的免疫原性问题并增强其兼容性。
2024年3月15日(当地时间),复旦大学基础医学院应天雷/吴艳玲团队在Acta pharmaceutica Sinica. B上发表了一篇名为“Single-domain antibodies as therapeutics for solid tumor treatment”的文章。该文章对sdAbs进行了全面的探讨,强调了它们的独特特点和人源化方法的进展。概述了基于sdAb的药物和治疗策略开发的最新进展及其在实体肿瘤治疗中的潜力,例如sdAb-药物偶联物、多特异性sdAb、基于sdAb的递送系统和基于sdAb的细胞疗法。

全人抗体是一类完全由人类自身序列组成的抗体。由于不存在其他异质序列,全人抗体被认为是非免疫原性的,不需要人源化,适合长期用作体内治疗剂,尤其是在治疗不同类型的癌症方面。目前已开发出多种方法来产生全人抗体,例如噬菌体展示技术,单B细胞筛选,另一种产生全人抗体的重要方法是使用免疫球蛋白(Ig)位点修饰的转基因小鼠。将小鼠的Ig基因替换为人类的基因,该转基因小鼠在免疫目标抗原后可以产生全人抗体。随着结构生物学的快速发展和大量蛋白质结构数据的出现,基于计算的抗体人源化方法也已通过同源性建模或人工智能(AI)被设计出来,用于生成人源化甚至完全人源抗体。
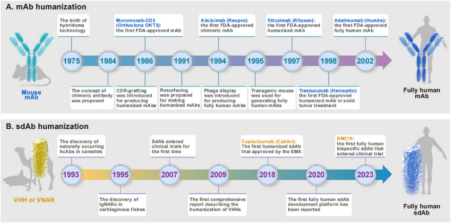
图 1 抗体发展示意图
sdAb具有体积小、稳定性好等显著特点,易于工程化,因此非常适合与其他蛋白和效应域融合,可同时作用于肿瘤部位,以获得更好的治疗效果。根据抗体修饰策略不同及与sdAb偶联的不同融合部分,抗肿瘤sdAb主要可分为以下几类:通过将单链抗体与毒素、多肽和化学物质融合而形成的单链抗体-药物偶联物;具有不同抗原结合位点的多特异性单链抗体;使用纳米载体的单链抗体递送系统,以及基于单链抗体的细胞疗法,例如嵌合抗原受体(CAR)-T细胞疗法。
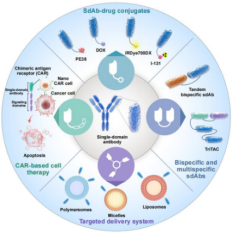
图2 用于实体瘤治疗的单域抗体的多种形式示意图
由于传统ADC的分子量较大,阻碍了其在实体肿瘤治疗中的应用,基于单链抗体的药物偶联物也称为纳米抗体-药物偶联物(NDC),是ADC由吸引力的替代品。与ADC类似,NDC可以通过智能接头将细胞毒性有效载荷与高亲和力单链抗体偶联,从而选择性杀死肿瘤细胞。由于单链抗体分子尺寸小,NDC能够以高亲和力结合抗原,并识别抗原上独特的隐藏表位,从而减少脱靶效应。该优势拓宽了单链抗体在实体肿瘤治疗中的应用,使其能够与多种类型的药物(如毒素、化疗化合物、光敏剂和治疗性放射性核素)联合使用。目前已有许多用于治疗实体肿瘤的已获批准或处于中后期临床试验的单克隆抗体药物。
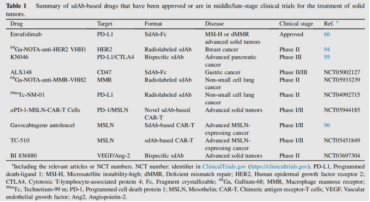
表1 已获批或处于实体瘤治疗中/后期临床试验阶段的单域抗体类药物汇总
综上所述,单域抗体凭借独特的理化性质和药理特性,在实体瘤治疗领域展现出巨大的应用潜力。随着人源化技术的不断优化、全人源单域抗体制备平台的完善以及多种治疗形式的持续研发,单域抗体有望为实体瘤患者带来更多新的治疗选择,推动实体瘤治疗领域迈向新的高度。未来,研究人员将继续致力于解决单域抗体在应用中存在的问题,如进一步优化其半衰期、提升靶向性等,为癌症治疗事业贡献更多力量。
复旦大学基础医学院应天雷教授、吴艳玲研究员为该论文的共同通讯作者,复旦大学基础医学院王铭楷博士为该论文的共同第一作者。
注:文中插图源于Acta pharmaceutica Sinica. B
相关研究:
