赋予抗体全新功能是生物医药领域的核心挑战。人工智能(AI)的快速发展为抗体智能化设计提供了强大驱动力,正在改变传统依赖随机突变与筛选的研究模式。单域抗体(sdAbs),其中包括来源于驼科动物的纳米抗体,凭借其小分子量、高稳定性及优异的组织穿透性,被认为是新一代生物治疗的重要平台。然而,在保持其原有抗原结合能力的前提下,精准赋予其全新功能,仍是科学界亟待攻克的关键难题。
2025年10月29日(当地时间),复旦大学应天雷团队与腾讯AI Lab姚建华团队于期刊Cell Discovery上发表了题为“A synergistic generative-ranking framework for tailored design of therapeutic single-domain antibodies”的研究论文。研究团队开发出基于深度学习的协同生成-排序AI模型TFDesign-sdAb,快速且精准地实现了单域抗体的功能定向生成,在实验验证中功能改造成功率达100%,为AI驱动的抗体理性设计和功能重塑提供了全新的解决方案。

模型创新:序列-结构协同的生成与筛选一体化设计
传统抗体工程方法,如噬菌体展示技术,流程繁琐、周期长、成功率低;现有的AI辅助设计方法多局限于互补决定区(CDRs)的优化,未能有效利用框架区(FRs)的功能潜力。
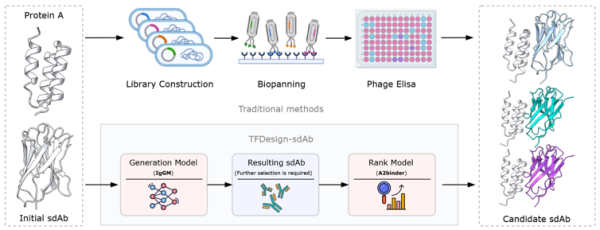
图1. 传统工程化技术与 TFDesign-sdAb在单域抗体功能改造流程的对比示意图
TFDesign-sdAb通过整合序列-结构协同扩散模型IgGM与亲和力排序模型A2binder,首次实现了抗体CDR与FR区域的协同设计。该模型不仅能在保留抗体原有抗原结合能力的前提下精准引入新功能,还能高效筛选出最具应用潜力的功能变体,大幅提升了设计效率与成功率。
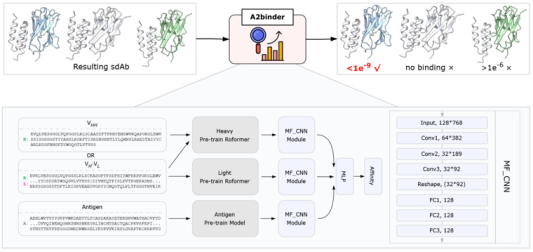
图2. A2binder 模型对单域抗体结合亲和力的预测流程及网络结构示意图
验证实例:赋予单域抗体Protein A 结合功能
为验证TFDesign-sdAb性能,研究团队以赋予单域抗体Protein A结合能力为目标展开系统验证。与传统单克隆抗体不同,单域抗体因缺乏Fc结构域,使其丧失了与Protein A结合能力,导致大规模生产中无法利用工业标准的Protein A亲和层析技术进行无标签纯化,极大限制了其规模化生产与临床转化。
针对3个人源单域抗体(n622、n67、n118)和1个驼源纳米抗体(VHH3),TFDesign-sdAb成功实现了100%的功能改造成功率,每个抗体都获得了高亲和力结合Protein A的变体,能通过Protein A亲和层析高效纯化,且保留了和原始抗原的结合能力。高分辨率结构分析(1.49 Å和2.0 Å)进一步揭示了改造后的单域抗体通过框架区介导的保守结合基序与Protein A相互作用,其结合模式与天然Fc-Protein A相互作用高度相似,从结构层面验证了TFDesign-sdAb平台设计的准确性与可解释性。成功实现Protein A亲和纯化将显著简化生产工艺、降低生产成本,有望加速单域抗体药物的临床转化与应用推广。
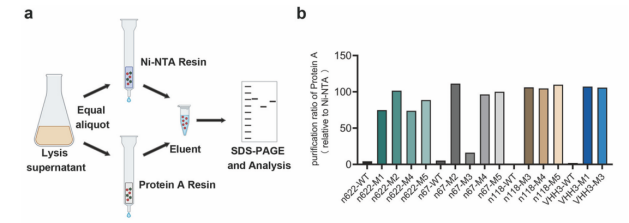
图3. 测试的单域抗体成功获得了通过Protein A亲和层析高效纯化的新功能
前景展望:面向多功能抗体设计的通用AI设计平台
作为一种通用性抗体设计平台,TFDesign-sdAb不止在于Protein A结合功能的改造,其核心框架可灵活拓展至抗体稳定性提升、半衰期延长、双特异性设计等多个领域,为多功能治疗性单域抗体的开发提供了普适工具。这项工作不仅验证了人工智能在解决蛋白质工程长期瓶颈问题中的核心价值,更标志着抗体研发范式的转变,从传统试错迈向AI驱动的理性设计,为快速开发功能增强的下一代治疗性全能单域抗体开辟了高效而精准的新路径。
复旦大学基础医学院应天雷教授、吴艳玲研究员、附属中山医院杨振霖研究员以及腾讯AI Lab姚建华教授为该文章的共同通讯作者,复旦大学上海市重大传染病和生物安全研究院助理研究员孔雨、硕士研究生赵婷、复旦大学基础医学院博士后史佳乐、腾讯AI Lab研究员吴凡迪、中国科学院微电子研究所博士研究生王儒博为该文章的共同第一作者。
注:文中插图源于 Cell Discovery
相关研究:
